Ένα θέμα που απασχόλησε αρκετά την επικαιρότητα πέρυσι δια μέσου (και) των έντονων τηλεοπτικών αντιπαραθέσεων μεταξύ Ιατρικών και Φαρμακευτικών Συλλόγων, ήταν αυτό της ηλεκτρονικής συνταγογράφησης με βάση τη δραστική ουσία, που εισήγαγε στην καθομιλουμένη τον όρο «γενόσημο φάρμακο» και μαζί μ’αυτόν μια ολόκληρη παραφιλολογία η οποία συχνά έφτανε στα όρια της επιστημονικής φαντασίας. Με πρόσφατη εγκύκλιό του το Υπουργείο Υγείας αναθέρμανε τη συζήτηση, πυροδοτώντας τις αντιδράσεις, αρχικά του ιατρικού σώματος στο ενδεχόμενο να αφαιρεθεί ολοκληρωτικά το δικαίωμα των γιατρών να καθορίζουν το εμπορικό σκεύασμα που προτιμούν να λάβει ο ασθενής τους και του φαρμακευτικού σώματος στη συνέχεια, όταν εκδόθηκε νεότερη εγκύκλιος που αναιρούσε τη ρύθμιση. Πολεμικές ανακοινώσεις εκατέρωθεν, μηνύσεις και σποραδικά επιστημονικά (ή επιστημονικοφανή) επιχειρήματα. Με αφορμή ορισμένες πολύ ενδιαφέρουσες συζητήσεις που διεξάγονται στα μέσα κοινωνικής δικτύωσης, θα επιχειρήσω μια σφαιρική αποτύπωση της κατάστασης, εξετάζοντας την από λίγο διαφορετική οπτική γωνία.
Ας ξεκινήσουμε με λίγη ορολογία.
Τι είναι τα γενόσημα φάρμακα;
Σύμφωνα με το European Medicines Agency, «γενόσημο είναι ένα φάρμακο που έχει αναπτυχθεί για να είναι το ίδιο με ένα φάρμακο που έχει ήδη άδεια κυκλοφορίας ( «φάρμακο αναφοράς»). Ένα γενόσημο φάρμακο περιέχει την ίδια δραστική ουσία ή ουσίες με το φάρμακο αναφοράς, και χρησιμοποιείται στην ίδια δόση για τη θεραπεία της ίδιας νόσου με το φάρμακο αναφοράς. Ωστόσο, το όνομά του, η εμφάνισή του (χρώμα ή σχήμα) και η συσκευασία του μπορεί να είναι διαφορετικές από εκείνες του φαρμάκου αναφοράς. Ένα γενόσημο φάρμακο περιέχει την ίδια ποσότητα της δραστικής ουσίας με το φάρμακο αναφοράς. Τα αδρανή συστατικά, ή «έκδοχα», μπορεί να διαφέρουν. Η δραστική ουσία του φαρμάκου είναι αυτή που του προσδίδει τη θεραπευτική του δράση. Ένας κατασκευαστής γενοσήμων μπορεί να χρησιμοποιήσει μια διαφορετική μορφή της δραστικής ουσίας, για παράδειγμα, ο κατασκευαστής μπορεί να αποφασίσει να χρησιμοποιήσει το υδροχλωρικό άλας της δραστικής ουσίας, επειδή αυτή η μορφή είναι πιο σταθερή. Ωστόσο, αυτό μπορεί μόνο να γίνεται εφόσον δεν επηρεάζει τη δραστικότητα του φαρμάκου»1.
Τι σημαίνει όμως «να είναι ίδιο με το το φάρμακο αναφοράς»; Σ’ αυτό το σημείο μπαίνουν στο παιχνίδι δύο νέοι όροι, η βιοδιαθεσιμότητα και η βιοϊσοδυναμία. Βιοδιαθεσιμότητα είναι το κλάσμα της χορηγούμενης δόσης που φτάνει αμετάβλητο στη συστηματική κυκλοφορία. Από τον ορισμό αυτό αμέσως γίνεται εμφανές ότι, αν και τα γενόσημα μπορεί να περιέχουν διαφορετικά έκδοχα, αυτό δεν έχει καμία σημασία, αφού το μέγεθος που μετράμε έχει υποστεί ήδη την όποια επίδραση των εκδόχων. Βιοϊσοδυναμία μεταξύ δύο σκευασμάτων είναι η απουσία σημαντικής διαφοράς κατά τη σύγκριση των βιοδιαθεσιμοτήτων τους.
Υπεισέρχονται όπως είναι φυσικό περισσότερες τεχνικές λεπτομέρειες σε αυτό το σημείο. Πολύ περιληπτικά, όπως αναφέρεται στις κατευθυντήριες οδηγίες για τη διερεύνηση της βιοϊσοδυναμίας της Επιτροπής Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση του EMA2, συγκρίνονται οι φαρμακοκινητικές παράμετροι AUC (0-t) ή ΑUC (0-72h) και C max . Η βιοϊσοδυναμία στοιχειοθετείται όταν οι λόγοι των γεωμετρικών μέσων των παραπάνω παραμέτρων έχουν 90% πιθανότητα να βρίσκονται εντός του διαστήματος 80-125% (90%-111% για τα φάρμακα στενού θεραπευτικού δείκτη). Προφανώς το παραπάνω δεν σημαίνει ότι ένα γενόσημο φάρμακο μπορεί να περιέχει 20% λιγότερη ή 25% περισσότερη δραστική ουσία από το πρωτότυπο, ή ότι η διαφορά στο κλινικό αποτέλεσμα είναι έως 45%, όπως λανθασμένα συνηθίζεται να λέγεται. Μία ανασκόπηση του FDA σε 2.070 μελέτες σε ανθρώπους από το 1996 έως το 20073, έδειξε ότι η μέση διαφορά στη βιοδιαθεσιμότητα μεταξύ γενόσημων και πρωτότυπων φαρμάκων ήταν μόλις 3,5%, με κάποια γενόσημα να εμφανίζουν ελαφρώς αυξημένη και άλλα ελαφρώς μειωμένη απορρόφηση. Σύμφωνα μάλιστα με τον FDA, μια τέτοια διαφορά είναι δικαιολογημένη και αναμενόμενη, δεν είναι κλινικά σημαντική και πολύ συχνά παρατηρείται και μεταξύ διαφορετικών παρτίδων ενός πρωτότυπου φαρμάκου. Προς επίρρωσιν του προηγούμενου, μία συστηματική ανασκόπηση και μετα-ανάλυση 47 μελετών που εξέτασαν κλινικά αποτελέσματα μεταξύ πρωτότυπων και γενόσημων καρδιολογικών φαρμάκων4, κατέληξε σε συμπέρασμα μη-ανωτερότητας των πρώτων.
Σε ό,τι αφορά την ποιότητά τους ως φαρμακευτικά προϊόντα, τα γενόσημα δεν υπόκεινται σε κάποια εξαίρεση. Οι κατασκευαστές γενοσήμων οφείλουν να τηρούν τους Κανόνες Καλής Παρασκευής και Διανομής όπως ακριβώς και οι κατασκευαστές πρωτοτύπων. Για την ακρίβεια, η μοναδική διαφορά στη διαδικασία αδειοδότησης ενός γενόσημου από ένα πρωτότυπο φάρμακο, είναι η μη-υποχρέωση του κατασκευαστή γενοσήμων να υποβάλλει μελέτες κλινικής αποτελεσματικότητας σε ζώα και ανθρώπους αλλά μελέτες βιοϊσοδυναμίας στη θέση τους.
Ανακεφαλαιώνοντας τα μέχρι τώρα δεδομένα, μπορούμε να διατυπώσουμε την πρώτη μας παραδοχή:
Α. Τα γενόσημα φάρμακα, ως κατηγορία φαρμακευτικών προϊόντων, είναι το ίδιο ασφαλή και αποτελεσματικά με τα πρωτότυπα φάρμακα, η δε χρήση τους επιτρέπει πολύ σημαντική εξοικονόμηση πόρων (υπολογίζεται σε 35 δις ευρώ η ετήσια εξοικονόμηση μόνο για την Ευρώπη).
Το κυρίαρχο επιχείρημα των Ιατρικών Συλλόγων είναι πως, καθώς ο γιατρός έχει την ευθύνη για τη θεραπεία του ασθενή (σωστό), πρέπει να έχει και την αποκλειστική ευθύνη της επιλογής συγκεκριμένου εμπορικού σκευάσματος. Για να προσδώσουν επιστημονικό έρεισμα στον ισχυρισμό τους, αναφέρουν την πολύπαθη «κλινική εμπειρία» ως κριτήριο αξιολόγησης της αποτελεσματικότητας ενός φαρμάκου. Θεωρούν δηλαδή πως ο γιατρός, μέσα από τα 5 ή 10 ή 50 ή 100 συγκρίσιμα (;) περιστατικά που έχει συναντήσει στην καριέρα του, έχει τη δυνατότητα να αποφανθεί για την κλινική αποτελεσματικότητα κάθε φαρμάκου που έχει τύχει να χρησιμοποιήσει. Δεν πρόκειται να επεκταθώ ιδιαίτερα σε αυτό το σημείο, καθώς θεωρώ ότι δεν αντέχει σε σοβαρή κριτική. Θα αρκεστώ να πω ότι η προσωπική εμπειρία είναι εκ των πραγμάτων biased και τα ανεκδοτολογικά στοιχεία δεν προκρίνονται ως evidence, ειδικά σε μια εποχή που η Ιατρική αναγνωρίζεται ως επιστήμη και όχι ως τέχνη. Ο μόνος τρόπος να αξιολογηθεί η κλινική αποτελεσματικότητα των φαρμάκων είναι η πειραματική μέθοδος και δεν χωράνε υποσημειώσεις και αστεράκια σε αυτό.
Ας ανανεώσουμε τη λίστα των παραδοχών μας λοιπόν:
Α. Τα γενόσημα φάρμακα, ως κατηγορία φαρμακευτικών προϊόντων, είναι το ίδιο ασφαλή και αποτελεσματικά με τα πρωτότυπα φάρμακα, η δε χρήση τους επιτρέπει πολύ σημαντική εξοικονόμηση πόρων (υπολογίζεται σε 35 δις ευρώ η ετήσια εξοικονόμηση μόνο για την Ευρώπη).
Β. Ο Ιατρός δεν έχει καμία επιστημονική νομιμοποίηση να αποφαίνεται για την κλινική αποτελεσματικότητα συγκεκριμένων εμπορικών σκευασμάτων, με βάση την κλινική του εμπειρία και μόνο. Το επιτυχημένο marketing των εταιρειών δεν είναι απαραίτητα συνώνυμο με την επιστημονική μέθοδο.
Λιγότερο χρόνο θα αφιερώσω για να απορρίψω το ίδιο επιχείρημα από την πλευρά των Φαρμακοποιών. Λένε δηλαδή ότι, καθώς έχουμε σπουδάσει το φάρμακο, είμαστε οι καθ’ ύλην αρμόδιοι να αποφαινόμαστε για την αποτελεσματικότητα του κάθε σκευάσματος. Συγγνώμη που θα σας απογοητεύσω συνάδελφοι, αλλά δεν είναι έτσι. Αποτελεί τεράστιο άλμα λογικής και καλά θα κάνετε να το εγκαταλείψετε. Ισχύει το πείραμα. Μόνο. Τίποτα άλλο.
Η λίστα των παραδοχών μας τροποποιείται λιγάκι:
Α. Τα γενόσημα φάρμακα, ως κατηγορία φαρμακευτικών προϊόντων, είναι το ίδιο ασφαλή και αποτελεσματικά με τα πρωτότυπα φάρμακα, η δε χρήση τους επιτρέπει πολύ σημαντική εξοικονόμηση πόρων (υπολογίζεται σε 35 δις ευρώ η ετήσια εξοικονόμηση μόνο για την Ευρώπη).
Β. Ούτε ο Ιατρός ούτε ο Φαρμακοποιός έχουν την επιστημονική νομιμοποίηση να αποφαίνονται για την κλινική αποτελεσματικότητα συγκεκριμένων εμπορικών σκευασμάτων, με βάση την κλινική τους εμπειρία ή τις θεωρητικές τους γνώσεις και μόνο. Το επιτυχημένο marketing των εταιρειών που καταφέρνει να πείσει είτε τον ένα είτε τον άλλον, δεν είναι απαραίτητα συνώνυμο με την επιστημονική μέθοδο.
Από τα παραπάνω προκύπτει εύκολα και η τρίτη παραδοχή:
Οποιοδήποτε γενόσημο φάρμακο κυκλοφορεί νόμιμα στην αγορά, με απόλυτη ευθύνη του ΕΟΦ, είναι κατάλληλο να χρησιμοποιηθεί ως πρώτη αγωγή σε ασθενή που ξεκινάει για πρώτη φορά θεραπεία και άρα θα ρυθμιστεί με αυτό.
Πράγμα που μας οδηγεί στο επόμενο σημείο που θα μας απασχολήσει.
Είδαμε πιο πάνω ότι η αλλαγή μεταξύ γενόσημου και πρωτότυπου, τις περισσότερες φορές, δεν συνοδεύεται από μεταβολή στο κλινικό αποτέλεσμα. Εξαίρεση αποτελούν τα φάρμακα στενού θεραπευτικού δείκτη, τα φάρμακα με πολύ «σφιχτή» σχέση μεταξύ δόσης και απόκρισης (πχ αντιεπιληπτικά, αντιψυχωτικά), τα εισπνεόμενα στεροειδή, οι ορμόνες και μερικές άλλες κατηγορίες, για τα οποία η γενική σύσταση είναι να αποφεύγονται οι αλλαγές. Όμως ενδέχεται να υπάρξει πρόβλημα όταν γίνεται αλλαγή ενός γενοσήμου με κάποιο άλλο. Αν και οι περισσότεροι κατασκευαστές γενοσήμων φροντίζουν ώστε οι βιοϊσοδυναμίες των προϊόντων τους να βρίσκονται κοντά στη μονάδα, υπάρχει πάντα η πιθανότητα κάποια φάρμακα να βρίσκονται στα 2 άκρα του διαστήματος 80%-125%. Τα φάρμακα αυτά, αν και βιοϊσοδύναμα ως προς το πρωτότυπο, είναι προφανές ότι δεν είναι βιοϊσοδύναμα μεταξύ τους και, ανάλογα με την περίπτωση, είναι πιθανό να προκληθούν παρενέργειες που σχετίζονται είτε με υπερδοσολογία είτε με υποθεραπευτική δόση. Ίσως είναι πιο κατανοητό αυτό, οπτικοποιημένο:
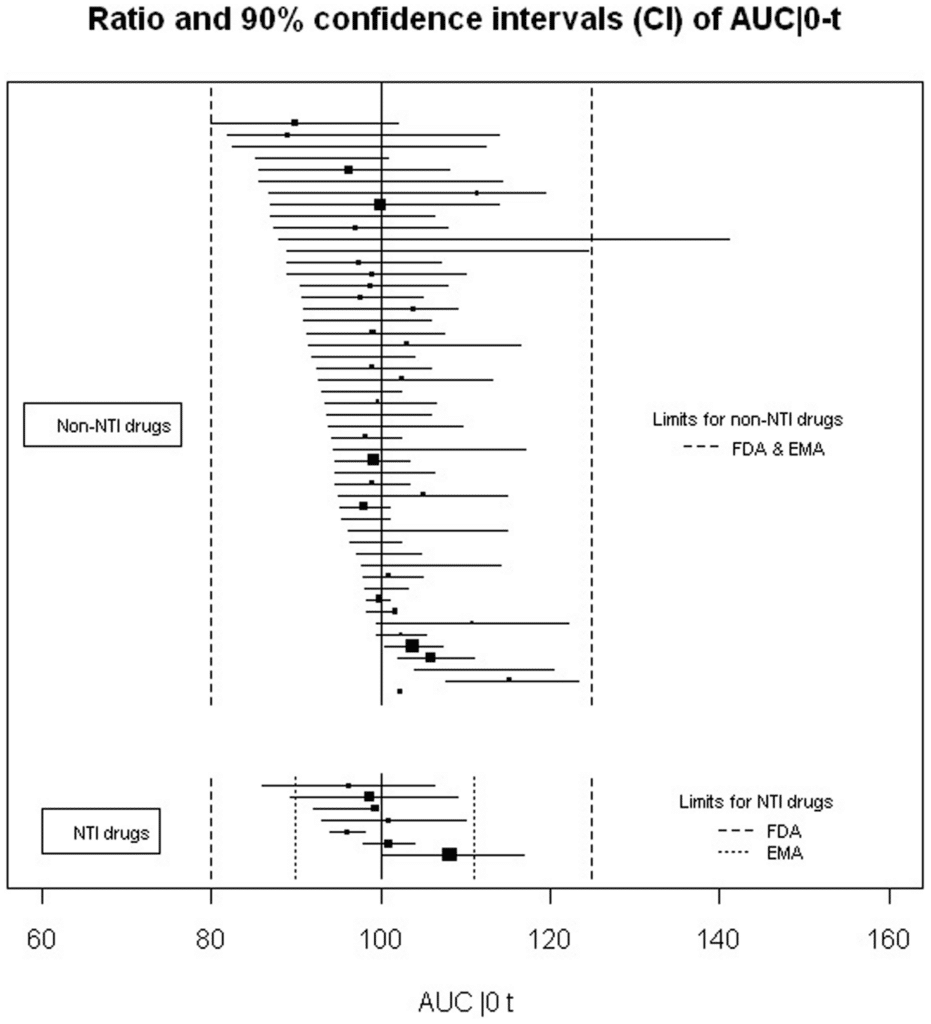
Όπως βλέπετε στις εικόνες, η πλειοψηφία των γενοσήμων έχουν φαρμακοκινητικές παραμέτρους των οποίων οι γεωμετρικοί μέσοι όροι βρίσκονται κοντά στη μονάδα, εντούτοις, δεν λείπουν οι outliers που μπορούν να δημιουργήσουν προβλήματα όταν γίνει αλλαγή από το ένα στο άλλο. Τα διαγράμματα προέρχονται από τη μελέτη “Quality of reporting of bioequivalence trials comparing generic to brand name drugs: a methodological systematic review”5 που δημοσιεύθηκε στο Plos ONE.
Ο μοναδικός τρόπος για να αντιμετωπιστεί αυτό το ενδεχόμενο λοιπόν, είναι η δημιουργία μιας βάσης δεδομένων που να περιέχει στοιχεία «θεραπευτικής ισοδυναμίας» για όλα τα φάρμακα της αγοράς. Αυτό ακριβώς κάνει το περίφημο Orange Book του FDA και η χρήση του έχει ως εξής: Ο ιατρός συνταγογραφεί δραστική ουσία (εκτός κι αν έχει συγκεκριμένο λόγο που επιλέγει πρωτότυπο σκεύασμα, οπότε και το αιτιολογεί πάνω στη συνταγή), και ο φαρμακοποιός που εκτελεί τη συνταγή είτε δίνει το ίδιο γενόσημο που παίρνει ο ασθενής είτε, αν δεν το έχει, συμβουλεύεται το orange book και δίνει το γενόσημο που βρίσκεται «πιο κοντά», ώστε να εξασφαλίσει έμμεση βιοϊσοδυναμία. Είναι προφανές ότι για λόγους φαρμακοοικονομίας είναι λογικό να κάνει την επιλογή ο φαρμακοποιός που επιβαρύνεται με τα κόστη διατήρησης του αποθέματός του και όχι ο γιατρός. Ο τελευταίος ενημερώνεται από το φαρμακοποιό για το ακριβές φάρμακο που πήρε ο ασθενής του και όλοι είναι χαρούμενοι: ο γιατρός γιατί ξέρει πως ο ασθενής του πήρε βιοϊσοδύναμο φάρμακο, ο ασθενής για τον ίδιο λόγο, ο φαρμακοποιός γιατί αξιοποίησε το ήδη αγορασμένο απόθεμά του και ο FDA γιατί γνωρίζει ότι με αυτό τον τρόπο κόβεται η σύνδεση ανάμεσα σε γιατρούς και φαρμακευτικές εταιρίες.
Πάμε λοιπόν, κλείνοντας, να ολοκληρώσουμε τη λίστα των παραδοχών μας:
Α. Τα γενόσημα φάρμακα, ως κατηγορία φαρμακευτικών προϊόντων, είναι το ίδιο ασφαλή και αποτελεσματικά με τα πρωτότυπα φάρμακα, η δε χρήση τους επιτρέπει πολύ σημαντική εξοικονόμηση πόρων (υπολογίζεται σε 35 δις ευρώ η ετήσια εξοικονόμηση μόνο για την Ευρώπη).
Β. Ούτε ο Ιατρός ούτε ο Φαρμακοποιός έχουν την επιστημονική νομιμοποίηση να αποφαίνονται για την κλινική αποτελεσματικότητα συγκεκριμένων εμπορικών σκευασμάτων, με βάση την κλινική τους εμπειρία ή τις θεωρητικές τους γνώσεις και μόνο. Το επιτυχημένο marketing των εταιρειών που καταφέρνει να πείσει είτε τον ένα είτε τον άλλον, δεν είναι απαραίτητα συνώνυμο με την επιστημονική μέθοδο.
Γ. Οποιοδήποτε γενόσημο φάρμακο κυκλοφορεί νόμιμα στην αγορά, με απόλυτη ευθύνη του ΕΟΦ, είναι κατάλληλο να χρησιμοποιηθεί ως πρώτη αγωγή σε ασθενή που ξεκινάει για πρώτη φορά θεραπεία και άρα θα ρυθμιστεί με αυτό.
Δ. Ο μοναδικός τρόπος να εξασφαλιστεί πως οι ασθενείς λαμβάνουν βιοϊσοδύναμα σκευάσματα σε περιπτώσεις αλλαγής μεταξύ γενοσήμων, είναι η δημιουργία μιας ανοικτής βάσης δεδομένων με τις μελέτες βιοϊσοδυναμίας όλων των προϊόντων που κυκλοφορούν στην αγορά, στα πρότυπα του Orange Book του FDA. Για λόγους οικονομίας, είναι πιο λογικό να κάνει την επιλογή ο φαρμακοποιός κατά την εκτέλεση της συνταγής, με ταυτόχρονη ενημέρωση του γιατρού από το σύστημα, ως δικλείδα ασφαλείας και ελέγχου.
Οι παραδοχές αυτές στηρίζονται σε επιστημονικά δεδομένα. Οι όποιες ενστάσεις υπάρχουν για τον τρόπο καθορισμού της βιοϊσοδυναμίας των γενοσήμων φαρμάκων, αφενός αποτελούν αντικείμενο συζήτησης και εκτός Ελλάδας και, αφετέρου, είναι αντικείμενο των Οργανισμών που καθορίζουν την πολιτική φαρμάκου σε υπερ-εθνικό επίπεδο και όχι ατομικά του κάθε επαγγελματία υγείας ή ακόμα και του Συλλόγου που αυτός ανήκει. Πρέπει να κατανοήσουμε όλοι ότι είναι αδιανόητο να επισκιάζουν τα συμφέροντα των επαγγελματιών υγείας, είτε οικονομικά είτε γοήτρου, αυτά των ασθενών, σε μία χώρα που επιθυμεί να ανήκει στον πολιτισμένο κόσμο.
ΑΝΑΦΟΡΕΣ
- European Medicines Agency, 2012. Questions and answers on generic medicines. EMA/393905/2006 Rev. 2
- COMMITTEE FOR MEDICINAL PRODUCTS FOR HUMAN USE/EMA, 2010. GUIDELINE ON THE INVESTIGATION OF BIOEQUIVALENCE. CPMP/EWP/QWP/1401/98 Rev. 1
- Davit BM, Nwakama PE, Buehler GJ, Conner DP, Haidar SH, Patel DT, Yang Y, Yu LX, Woodcock J. Comparing generic and innovator drugs: a review of 12 years of bioequivalence data from the United States Food and Drug Administration. Ann Pharmacother. 2009 Oct;43(10):1583-97. doi: 10.1345/aph.1M141. Epub 2009 Sep 23. PubMed PMID: 19776300.
- Kesselheim AS, Misono AS, Lee JL, et al. Clinical Equivalence of Generic and Brand-Name Drugs Used in Cardiovascular Disease: A Systematic Review and Meta-analysis. JAMA. 2008;300(21):2514-2526. doi:10.1001/jama.2008.758.
- van der Meersch A, Dechartres A, Ravaud P. Quality of reporting of bioequivalence trials comparing generic to brand name drugs: a methodological systematic review. PLoS One. 2011;6(8):e23611. doi: 10.1371/journal.pone.0023611. Epub 2011 Aug 17. Review. PubMed PMID: 21858184; PubMed Central PMCID: PMC3157430.