*Του Ρωμανού Σκλαβενίτη-Πιστοφίδη
Επικαιροποιήθηκε στις 7 Σεπτεμβρίου 2016.
Εισαγωγή
To 2016, o αριθμός των HIV+ ατόμων υπό cART (συνδυασμένη αντιρετροϊκή αγωγή) έφτασε τα 17 εκατομμύρια [1]· 2 εκατομμύρια πάνω από τον αρχικό στόχο, που ήθελε 15 εκατομμύρια HIV+ ατόμων υπό αγωγή μέχρι το 2015 («15 μέχρι το ’15»). Η cART έχει αντίκτυπο τόσο στην ατομική όσο και στη δημόσια υγεία: αφενός, τροποποιεί τη φυσική ιστορία της νόσου (η χρόνια HIV λοίμωξη υπό cART είναι πια μία ανίατη, χρόνια νόσος με υπό όρους κανονικό προσδόκιμο ζωής [2]) και αφετέρου, περιορίζει τη σεξουαλική μετάδοση του HIV-1¹ [3]. Ωστόσο, ο χρόνος έναρξης της θεραπείας συνιστά αμφιλεγόμενο ζήτημα υπό διερεύνηση: οι εθνικές κατευθυντήριες οδηγίες μπορεί να μην ταυτίζονται μεταξύ τους, αλλά ούτε και με εκείνες του Παγκόσμιου Οργανισμού Υγείας (Π.Ο.Υ.) ή άλλων task forces. Αυτό, διότι ενώ είναι αδιαμφισβήτητο ότι πρέπει να λάβουν θεραπεία HIV+ άτομα με προχωρημένη λοίμωξη, κακή κλινική ή εργαστηριακή εικόνα, υπάρχουν αμφιβολίες σε ό,τι αφορά τα υπόλοιπα HIV+ άτομα, δηλαδή εκείνα που έχουν μόλις διαγνωστεί, είναι ασυμπτωματικά και διατηρούν καλή εργαστηριακή εικόνα. Καθώς, όμως, προκύπτουν νέα δεδομένα, ενισχύεται η τάση για την ολοένα και νωρίτερα έναρξη cART, ενδεχομένως και κατά τη διάγνωση.

Ζητήματα ορολογίας: HIV λοίμωξη VS. AIDS
Παρότι συνηθίζεται οι δύο όροι, «HIV λοίμωξη» και «AIDS», να χρησιμοποιούνται εναλλάξ από την κοινή γνώμη, στην πραγματικότητα αποτελούν σχετιζόμενες διακριτές οντότητες. Επιπλέον, ο όρος «HIV λοίμωξη» υποδηλώνει τη Χρόνια Εγκατεστημένη HIV Λοίμωξη και πρέπει να διακρίνεται τόσο από το AIDS (Σύνδρομο Επίκτητης Ανοσοανεπάρκειας) όσο και από την Οξεία HIV Λοίμωξη.
Η Οξεία HIV Λοίμωξη εκδηλώνεται 1 με 3 εβδομάδες μετά τη μόλυνση ως γριππώδης συνδρομή ή σύνδρομο λοιμώδους μονοπυρήνωσης2, που μπορεί να συνοδεύεται από εξάνθημα και νευρολογικές εκδηλώσεις και διαρκεί 1 με 12 εβδομάδες. Από την άλλη, βάσει της σταδιοποίησης που προτείνει ο Π.Ο.Υ. [4], η Χρόνια Εγκατεστημένη HIV Λοίμωξη διακρίνεται σε τέσσερα κλινικά στάδια, καθένα από τα οποία ορίζεται από διαφορετικές νοσολογικές οντότητες (για παράδειγμα η παρουσία γωνιακής χειλίτιδας, που δεν μπορεί να αποδοθεί σε έλλειψη σιδήρου ή βιταμινών, ορίζει στάδιο 2, ενώ η παρουσία πνευμονικής φυματίωσης στάδιο 3). Από αυτά, μόνο το στάδιο 4 ισοδυναμεί με AIDS. Σημειωτέον πως η διάγνωση του AIDS σε ενήλικες μπορεί να τεθεί είτε κλινικά (σε πιθανή ή διαπιστωμένη παρουσία οντότητας που ορίζει κλινικό στάδιο 4) είτε εργαστηριακά (την πρώτη φορά που τα CD4+ T-λεμφοκύτταρα είναι <200/mm³ ή <15%).
CD4+ Τ-λεμφοκύτταρα και HIV
Τα Τ-λεμφοκύτταρα διακρίνονται σε 4 κύριους τύπους: βοηθητικά, κυτταροτοξικά, μνήμης και ρυθμιστικά Τ-λεμφοκύτταρα. Καθένας απ’ αυτούς φέρει στην επιφάνειά του ειδικούς δείκτες διαφοροποίησης, γνωστούς ως CD (Cluster of Differentiation)· αυτοί οι δείκτες καθορίζουν τον ανοσοφαινότυπο του κυττάρου, τον οποίο μπορούμε να αναγνωρίσουμε με την κυτταρομετρία ροής. Έτσι, όλα τα Τ-λεμφοκύτταρα είναι CD3+ (φέρουν, δηλαδή, τον δείκτη CD3 στην επιφάνειά τους), τα βοηθητικά Τ-λεμφοκύτταρα είναι CD3+ και επιπλέον CD4+, τα κυτταροτοξικά Τ-λεμφοκύτταρα είναι CD3+ και επιπλέον CD8+ κ.λπ. Ένα κύτταρο λοιπόν θετικό για τους δείκτες CD3 και CD4 είναι ένα βοηθητικό Τ-λεμφοκύτταρα ή CD4+ Τ-λεμφοκύτταρο.
Το CD4 μόριο αποτελεί τον κύριο υποδοχέα του HIV· δηλαδή, ο HIV μολύνει μόνον CD4+ κύτταρα. Στην πλειονότητά τους, αυτά είναι τα CD4+ T-λεμφοκύτταρα, αν και CD4 μόριο μπορεί να υπάρχει στην επιφάνεια και άλλων κυττάρων, όπως για παράδειγμα των μακροφάγων. Αφού λοιπόν εισέλθει στα CD4+ Τ-λεμφοκύτταρα, ο HIV τα καταστρέφει είτε άμεσα είτε έμμεσα με πολύπλοκους ανοσολογικούς μηχανισμούς και καθώς είναι απαραίτητα για την εύρυθμη λειτουργία του ανοσοποιητικού συστήματος, οδηγεί σε ανοσοανεπάρκεια. Ο βαθμός καταστροφής των CD4+ T-λεμφοκυττάρων αποτελεί ένα μέτρο εξέλιξης της νόσου: όσο ο ιός πολλαπλασιάζεται τόσο περισσότερα CD4+ T-λεμφοκύτταρα καταστρέφονται και τόσο επιδεινώνεται η ανοσοανεπάρκεια.
Έναρξη cART: οι οδηγίες
Στην παρακολούθηση των HIV+ ατόμων, οι χρησιμότερες παράμετροι είναι ο απόλυτος αριθμός των CD4+ Τ-λεμφοκυττάρων ανά κυβικό χιλιοστό, ελλείψει του οποίου μπορεί να χρησιμοποιηθεί το αντίστοιχο ποσοστό, και το ιικό φορτίο που μετράται σε αντίγραφα/ml. Το ιικό φορτίο δεν χρησιμοποιείται κατά κανόνα στον καθορισμό του χρόνου έναρξης της θεραπείας, αλλά περισσότερο ως ένδειξη ανταπόκρισης στη θεραπεία ή θεραπευτικής αποτυχίας και ως προγνωστικός παράγοντας. Παρόλ’ αυτά, καθώς το ιικό φορτίο αποτελεί δείκτη ενεργότητας του ιού, υψηλές τιμές φορτίου (>100.000 αντίγραφα/ml ή κατ’ άλλους, >55.000 αντίγραφα/ml) σε ασθενείς με υψηλές τιμές CD4+ Τ-λεμφοκυττάρων (που, βάσει των οδηγιών, δεν δικαιολογούν έναρξη θεραπείας) μπορεί κατά περίπτωση να θέσουν ένδειξη έναρξης θεραπείας [5,6], ακόμη κι αν δεν υπάρχει σχετική εμπεριστατωμένη οδηγία.
Καθότι τα 2/3 των HIV+ ασθενών κατοικούν στην Αφρική, όπου οι υπηρεσίες υγείας περιορίζονται έντονα από το κόστος, η παρακολούθηση των οροθετικών ατόμων με τακτικό έλεγχο των CD4+ Τ-λεμφοκυττάρων τους δεν είναι πάντοτε εφικτή, με αποτέλεσμα να καθυστερεί η έναρξη της αντιρετροϊκής θεραπείας με δυσμενείς συνέπειες για την υγεία των ατόμων, αλλά και τη δημόσια υγεία. Προκειμένου λοιπόν να ξεπεραστεί τυχόν οικονομική δυσπραγία, ο Π.Ο.Υ. καθόρισε και κλινικά κριτήρια για την έναρξη της cART, ενώ σε τέτοιες περιπτώσεις, αντί του αριθμού CD4+ T-λεμφοκυττάρων που υπολογίζεται μέσω κυτταρομετρίας ροής, μπορεί να χρησιμοποιηθεί ο Απόλυτος Αριθμός Λεμφοκυττάρων, που υπολογίζεται από μια απλή Γενική Αίματος. Ας σημειωθεί ότι συνεκτίμηση της κλινικής εικόνας συστήνεται ακόμη και σε περιπτώσεις που η μέτρηση των CD4+ Τ-λεμφοκυττάρων είναι υπόθεση ρουτίνας.
Όπως είναι φυσικό, οι οδηγίες για τον χρόνο έναρξης της θεραπείας ανανεώνονται κάθε λίγα χρόνια και η πορεία ενημέρωσής τους είναι διαφωτιστική. Στις πρώτες οδηγίες που εκδίδει ο Π.Ο.Υ. το 2002 [5], οι ασθενείς διακρίνονται σε ασυμπτωματικούς και συμπτωματικούς· η κλινική εικόνα, δηλαδή, αποτελεί την κύρια παράμετρο της απόφασης για έναρξη θεραπείας. Απόλυτος αριθμός CD4+ Τ-λεμφοκυττάρων ≤ 200/mm³ (τιμή που συμπίπτει με το κλινικό στάδιο 4 κατά WHO ή κλινικό στάδιο 3 κατά CDC [7], δηλαδή το AIDS) θεωρείται απόλυτη ένδειξη, ενώ συστήνεται εκτίμηση για έναρξη σε υψηλότερες τιμές. Κλινικές ενδείξεις αποτελούν εδώ το AIDS, ο παρατεινόμενος πυρετός για >2 εβδομάδες και η στοματική καντιντίαση (σημειωτέον πως οι δύο τελευταίες οντότητες αποτελούν σήμερα εκδηλώσεις του κλινικού σταδίου 3 κατά WHO), ανεξαρτήτως του αριθμού των CD4+ Τ-λεμφοκυττάρων ή του ιικού φορτίου. Έναρξη θεραπείας συστήνεται επίσης σε άτομα που έχουν CD4+ >350/mm³ και ταυτόχρονα ιικό φορτίο >55.000 αντίγραφα/ml. Τέλος, αφιερώνεται ειδικό κεφάλαιο στην έναρξη θεραπείας κατά την Οξεία HIV Λοίμωξη, όπου σημειώνεται η έλλειψη επιστημονικών αποδείξεων που να την υποστηρίζουν, ενώ εναποτίθεται στον θεράποντα ιατρό και τον ασθενή να ζυγίσουν το κόστος και τα οφέλη από πιθανή έναρξη της θεραπείας τόσο νωρίς στην πορεία της λοίμωξης.
Πράγματι, όπως αναγράφεται στις οδηγίες του 2002, η cART έχει και μειονεκτήματα. Χαρακτηριστικά, καθώς η θεραπεία λαμβάνεται εφ’ όρου ζωής, η συμμόρφωση των ασθενών στη θεραπεία είναι επισφαλής, ενώ υπάρχει κίνδυνος ανάπτυξης ανθεκτικών στελεχών του ιού. Επιπλέον, σημειώνεται πως όσο νωρίτερα αρχίσει η θεραπεία τόσο νωρίτερα μπορεί να εξαντληθεί η αποτελεσματικότητά της, με κίνδυνο να μην υπάρχουν εναλλακτικές θεραπευτικές επιλογές και ο ασθενής να καταλήξει σε σχετικά μικρή ηλικία. Τέλος, η cART έχει και σημαντικές παρενέργειες, όπως η χαρακτηριστική λιποδυστροφία [Εικόνα Ι] και η αντίσταση στην ινσουλίνη (φαρμακογενής σακχαρώδης διαβήτης).
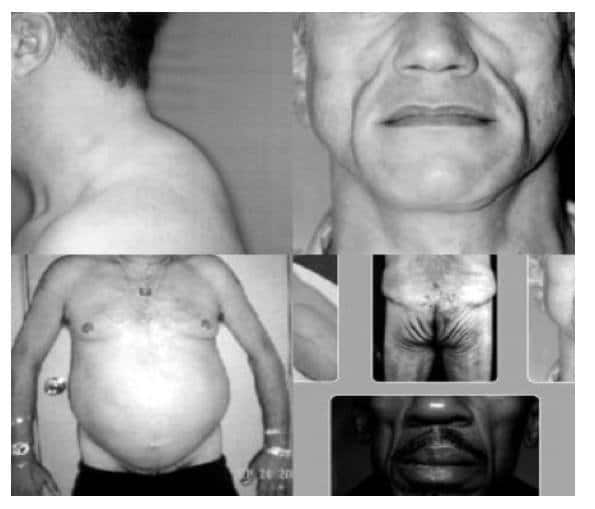
Με τις οδηγίες του 2002, λοιπόν, τίθεται το κατώτατο όριο έναρξης της θεραπείας (CD4+ ≤ 200/mm³), συμπεριλαμβάνονται κλινικές εκδηλώσεις σταδίου 3 στις ενδείξεις και συζητώνται εκτενώς τα προβλήματα που συνοδεύουν την πρώιμη έναρξη της cART.
Οι οδηγίες αυτές ενημερώνονται για πρώτη φορά το 2003. Στις νέες οδηγίες [8], αναγράφονται ξεχωριστά κριτήρια για τις περιπτώσεις όπου ο έλεγχος των CD4+ Τ-λεμφοκυττάρων είναι εφικτός και ξεχωριστά για εκείνες όπου δεν είναι. Όταν ο έλεγχος είναι εφικτός, η έναρξη της θεραπείας συστήνεται σε: i) Κλινικό Στάδιο 4, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων, ii) Κλινικό Στάδιο 3, όταν CD4+ <350/mm³ και iii) Κλινικό Στάδιο 1 ή 2, όταν CD4+ ≤200/mm³. Όταν δεν είναι εφικτός, ο απόλυτος αριθμός των CD4+ Τ-λεμφοκυττάρων υποκαθίσταται από τον Απόλυτο Αριθμό Λεμφοκυττάρων. Έτσι, η έναρξη της θεραπείας συστήνεται σε: i) Κλινικό Στάδιο 4, ανεξαρτήτως Απόλυτου Αριθμού Λεμφοκυττάρων, ii) Κλινικό Στάδιο 3, ανεξαρτήτως Απόλυτου Αριθμού Λεμφοκυττάρων και iii) Κλινικό Στάδιο 2, όταν Απόλυτος Αριθμός Λεμφοκυττάρων ≤1200/mm³. Καθώς ο Απόλυτος Αριθμός Λεμφοκυττάρων δεν είναι αξιόπιστος δείκτης σε ασυμπτωματικά HIV+ άτομα, όταν το άτομο είναι ασυμπτωματικό (Κλινικό Στάδιο 1 κατά WHO) και ο έλεγχος των CD4+ Τ-λεμφοκυττάρων δεν είναι εφικτός, δεν συστήνεται έναρξη θεραπείας.
Η επόμενη ενημέρωση των οδηγιών γίνεται το 2006 [9]. Σε αυτές, αναγνωρίζοντας το κόστος του τακτικού ελέγχου των ασθενών με κυτταρομετρία ροής, ο Π.Ο.Υ. προτείνει και πάλι κλινικά κριτήρια για την έναρξη της θεραπείας, ώστε αυτή να μην καθυστερεί όταν ο έλεγχος των CD4+ Τ-λεμφοκυττάρων δεν είναι εφικτός, ωστόσο υπογραμμίζει την αναγκαιότητα για ευρύτερη πρόσβαση σε εργαλεία ελέγχου και καλεί τα διάφορα εθνικά προγράμματα να ενσωματώσουν τη μέτρηση των CD4+ Τ-λεμφοκυττάρων στη ρουτίνα τους. Η έμφαση στη μέτρηση των CD4+ Τ-λεμφοκυττάρων αποτυπώνεται και στις οδηγίες, αφού για πρώτη φορά αντικαθιστούν την κλινική σταδιοποίηση ως κύρια παράμετρο, ενώ ξεχωριστή κατηγορία αφιερώνεται για πρώτη φορά στις εγκύους HIV+ ασθενείς και στη συλλοίμωξη με Μυκοβακτηρίδιο Φυματίωσης. Εδώ, έναρξη θεραπείας συστήνεται σε: i) CD4+ <200/mm³, ανεξαρτήτως Κλινικού Σταδίου, ii) 200/mm³< CD4+ <350/mm³, όταν Κλινικό Στάδιο 4 ή σοβαρές καταστάσεις Κλινικού Σταδίου 3 (Πνευμονική Φυματίωση, Σοβαρές Βακτηριακές Λοιμώξεις), ενώ δεν συστήνεται έναρξη θεραπείας για CD4+ > 350/mm³.
Εναλλακτικές οδηγίες με κύρια παράμετρο την κλινική σταδιοποίηση συνοδεύουν τις πρώτες και διακρίνονται ανάλογα με τη δυνατότητα ελέγχου των CD4+ Τ-λεμφοκυττάρων. Όταν τέτοια δυνατότητα δεν υπάρχει, συστήνεται έναρξη της θεραπείας σε Κλινικό Στάδιο 4, Κλινικό Στάδιο 3, αλλά και Κλινικό Στάδιο 2, υπό τον όρο ο Απόλυτος Αριθμός Λεμφοκυττάρων να είναι ≤ 1200/mm³. Αν δεν υπάρχει ούτε δυνατότητα υπολογισμού του Απόλυτου Αριθμού Λεμφοκυττάρων, τότε ασθενείς σε Κλινικό Στάδιο 2 δεν έχουν ένδειξη έναρξης θεραπείας. Όταν υπάρχει δυνατότητα ελέγχου των CD4+ Τ-λεμφοκυττάρων, συστήνεται έναρξη θεραπείας σε: i) Κλινικό Στάδιο 1 ή 2, όταν CD4+ ≤ 200/mm³, ii) Κλινικό Στάδιο 3, όταν CD4+ < 350/mm³, αλλά προτού φτάσουν τα 200/mm³ και iii) Κλινικό Στάδιο 4, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων.
Σε ό,τι αφορά τις Εγκύους HIV+ ασθενείς, έναρξη θεραπείας συστήνεται σε: i) Κλινικό Στάδιο 1 ή 2 και CD4+ ≤ 200/mm³, ii) Κλινικό Στάδιο 3, όταν CD4+ ≤350/mm³ και iii) Κλινικό Στάδιο 4, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων. Ενώ σε ό,τι αφορά τους HIV+ ασθενείς με συλλοίμωξη με Μυκοβακτηρίδιο Φυματίωσης, έναρξη θεραπείας συστήνεται όταν υπάρχει ενεργός Φυματίωση και CD4+ ≤ 350/mm³, ωστόσο σημειώνεται πως εφόσον CD4+ ≥200/mm³, η έναρξη της θεραπείας μπορεί να καθυστερήσει.
Ήδη στις οδηγίες του 2006, αποτυπώνονται οι τάσεις για πρωιμότερη έναρξη της θεραπείας. Το κατώφλι των 350/mm³ CD4+ Τ-λεμφοκυττάρων μπορεί να χρησιμοποιηθεί όταν συνυπάρχουν καταστάσεις Κλινικού Σταδίου 3, ιδιαίτερα αν πρόκειται για πνευμονική Φυματίωση ή Σοβαρές Βακτηριακές Λοιμώξεις.
Η επόμενη ενημέρωση των οδηγιών γίνεται το 2010 [10]. Αυτή συστήνει έναρξη θεραπείας σε: i) CD4+ ≤ 350/mm³, ii) Κλινικό Στάδιο 1 ή 2 και CD4+ ≤ 350/mm³ και iii) Κλινικό Στάδιο 3 ή 4, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων. Επιπλέον, σε ό,τι αφορά τις Εγκύους HIV+ ασθενείς, συστήνεται έναρξη θεραπείας σε: i) CD4+ ≤ 350/mm³, ανεξαρτήτως Κλινικού Σταδίου και ii) Κλινικό Στάδιο 3 ή 4, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων. Σε ό,τι αφορά τους ασθενείς με συλλοίμωξη με Μυκοβακτηρίδιο Φυματίωσης, συστήνεται έναρξη θεραπείας όταν υπάρχει ενεργός Φυματίωση, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων, ενώ αφιερώνεται ειδικό κεφάλαιο στη συλλοίμωξη με HBV (Ιός Ηπατίτιδας Β): σε αυτούς τους ασθενείς, συστήνεται έναρξη αντιρετροϊκής θεραπείας, όταν χρειάζονται θεραπεία για την Ηπατίτιδα Β, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων.
Το κατώτατο όριο τίθεται πια στα 350/mm³ CD4+ T-λεμφοκύτταρα, ενώ οποιαδήποτε κατάσταση ορίζει Κλινικό Στάδιο 3 θέτει την ένδειξη για έναρξη της θεραπείας. Λιγότερο συντηρητικές είναι οι οδηγίες και σε ό,τι αφορά τις εγκύους HIV+ ασθενείς και τους ασθενείς με συλλοίμωξη με Μυκοβακτηρίδιο Φυματίωσης ή HBV.
Η δημοσίευση των αποτελεσμάτων της μελέτης HPTN 052 τοποθετεί τη συζήτηση για την πρώιμη έναρξη της αντιρετροϊκής θεραπείας και σε ένα ακόμη επίπεδο· αυτό της δημόσιας υγείας. Παρότι η μελέτη επρόκειτο να ολοκληρωθεί το 2015, τα ευρήματά της είναι τόσο σημαντικά που διακόπτεται πρόωρα και τα αποτελέσματά της δημοσιεύονται το 2011 [3]. H μελέτη αυτή αποδεικνύει ότι η πρώιμη έναρξη cART μπορεί να προλάβει τη σεξουαλική μετάδοση του HIV-1. Την ίδια στιγμή, μελέτες παρατήρησης σημειώνουν πως η πρώιμη έναρξη θεραπείας αυξάνει την ελεύθερη-AIDS επιβίωση (AIDS-free survival) [11]. Αξιολογώντας αυτές τις εξελίξεις, το πάνελ ειδικών της Διεθνούς Αντι-ιικής Εταιρείας δημοσιεύει δικές του συστάσεις το 2012 [12], βάσει των οποίων ένδειξη για έναρξη αντιρετροϊκής θεραπείας έχουν όλα ανεξαιρέτως τα HIV+ άτομα. Τονίζεται ωστόσο πως η ποιότητα των αποδείξεων και άρα η ισχύς της σύστασης αυξάνεται καθώς ελαττώνεται ο αριθμός των CD4+ Τ-λεμφοκυττάρων. Ακόμη, υπογραμμίζεται η έλλειψη επαρκών πληροφοριών σε ό,τι αφορά τους λεγόμενους «ελίτ ρυθμιστές» και «μακράς διάρκειας μη εξελίξιμους» ασθενείς και την ασυμπτωματική Οξεία HIV Λοίμωξη, ενώ δίνεται έμφαση στη σημασία της ενημέρωσης του ασθενούς γύρω από τη θεραπεία, τα υπέρ και τα κατά της, την εκτίμηση της ετοιμότητάς του γι’ αυτή και της ικανότητάς του για συμμόρφωση.
Το 2013, ο Π.Ο.Υ. ενημερώνει και πάλι τις οδηγίες του [13,14]. Σε αυτές, συστήνεται έναρξη της θεραπείας σε όλους τους ασθενείς με CD4+ ≤ 500/mm³, αλλά συνιστάται έναρξη θεραπείας κατά προτεραιότητα σε ασθενείς με CD4+ ≤ 350/mm³ ή ασθενείς σε Κλινικό Στάδιο 3 ή 4. Επιπλέον, συστήνεται έναρξη θεραπείας, ανεξαρτήτως αριθμού CD4+ Τ-λεμφοκυττάρων και κλινικού σταδίου, σε ασθενείς με ενεργό Φυματίωση, συλλοίμωξη με HBV και σοβαρή χρόνια ηπατική νόσο, εγκύους ή θηλάζουσες4 HIV+ μητέρες και ΗΙV+ άτομα με οροαρνητικό/ή σύντροφο (για την ελάττωση του κινδύνου μετάδοσης).
Σημειωτέον πως εδώ συστήνεται για πρώτη φορά χορήγηση αντιρετροϊκής αγωγής για την πρόληψη της μετάδοσης, όμως ένδειξη γι’ αυτήν έχει μόνο το οροθετικό άτομο. Στις 14 Μαΐου 2014, το Κέντρο Ελέγχου και Πρόληψης Λοιμώξεων των Η.Π.Α. εκδίδει τις πρώτες οδηγίες για την Προ της Έκθεσης Προφύλαξη (PrEP: Pre-Exposure Prophylaxis) [15], όπου ένδειξη για αντιρετροϊκή αγωγή έχουν και HIV- ενήλικες, ομοφυλόφιλοι ή ετεροφυλόφιλοι, που βρίσκονται σε σχέση με οροθετικό/ή σύντροφο, ή δεν βρίσκονται σε μονογαμική σχέση με οροαρνητικό/ή σύντροφο, ή δεν χρησιμοποιούν πάντοτε προφυλακτικό στο πρωκτικό σεξ/ σεξ με άτομα αγνώστου HIV στάτους, ή εμφάνισαν κάποιο Σεξουαλικώς Μεταδιδόμενο Νόσημα τους τελευταίους 6 μήνες, ή επιδεικνύουν αμφιφυλοφιλική σεξουαλική συμπεριφορά (αφορά τους άνδρες) ή κάνουν σεξ με άνδρες που επιδεικνύουν αμφιφυλοφιλική σεξουαλική συμπεριφορά (αφορά τις γυναίκες).
Τον Ιούλιο του 2014, το πάνελ ειδικών της Διεθνούς Αντι-ιικής Εταιρείας ενημερώνει τις δικές του συστάσεις [16]. Επικαλούμενοι μελέτες παρατήρησης, την Τυχαιοποιημένη Κλινική Μελέτη HPTN 052, την έλλειψη στοιχείων που να αποδεικνύουν πως πρώιμη έναρξη θεραπείας μπορεί να βλάψει και μοντέλα κόστους-οφέλους (cost-effectiveness models), επιμένουν στη σύστασή τους για έναρξη αντιρετροϊκής θεραπείας σε όλα ανεξαιρέτως τα HIV+ άτομα, τονίζοντας πως η ποιότητα των αποδείξεων και άρα η ισχύς της σύστασης αυξάνονται καθώς ο αριθμός των CD4+ Τ-λεμφοκυττάρων ελαττώνεται. Συγκεκριμένα, η σύσταση είναι ισχυρότερη (τάξης ΑΙα) σε ό,τι αφορά ασθενείς με CD4+ ≤ 500/mm³ και ασθενέστερη (τάξης ΒΙΙΙ) σε ό,τι αφορά ασθενείς με CD4+ > 500/mm³. Ισχυρή (τάξης Α), ωστόσο, είναι και η σύσταση σε ό,τι αφορά ειδικές κατηγορίες ασθενών με CD4+ >500/mm³, όπως είναι οι έγκυοι γυναίκες, η συλλοίμωξη με HBV και η Σχετιζόμενη με HIV Νεφροπάθεια (σημειωτέον, πως η τελευταία ορίζει Κλινικό Στάδιο 4 κατά WHO). Έναρξη θεραπείας συστήνεται (τάξη ΒΙΙΙ) και κατά τη διάρκεια της Οξείας HIV Λοίμωξης, ενώ ένδειξη τίθεται και σε ασθενείς με ευκαιριακές λοιμώξεις ή άλλα Καθοριστικά του AIDS Νοσήματα3. Τέλος, συστήνεται έναρξη θεραπείας σε συλλοίμωξη με Μυκοβακτηρίδιο Φυματίωσης 2 εβδομάδες μετά την έναρξη της αντιφυματικής αγωγής, όταν CD4+ <50/mm³, αλλά μπορεί να καθυστερήσει για 8 με 12 εβδομάδες, όταν ο αριθμός CD4+ Τ-λεμφοκυττάρων είναι μεγαλύτερος.
2016: τα νεότερα δεδομένα
Τον Ιούνιο του 2016, στις ανανεωμένες οδηγίες του, ο Π.Ο.Υ. προτείνει την έναρξη cART σε όλα τα HIV+ άτομα, ανεξαρτήτως αριθμού CD4+ T-λεμφοκυττάρων και κλινικού σταδίου, εφόσον το άτομο κρίνεται έτοιμο να αναλάβει την ευθύνη της συμμόρφωσης στην εφ’ όρου ζωής θεραπεία [17]. Σημειώνεται, ωστόσο, ότι θεραπεία θα πρέπει να λάβουν κατά προτεραιότητα όσοι πάσχουν από νόσο κλινικού σταδίου 3 ή 4 ή έχουν αριθμό CD4+ T-λεμφοκυττάρων ≤ 350/mm3.
Παρότι η σύσταση είναι ισχυρή, τα δεδομένα που την υποστηρίζουν έχουν αδυναμίες. Οι συγκεκριμένες οδηγίες προέκυψαν με βάση μελέτες παρατήρησης (οι οποίες πρέπει πάντοτε να αντιμετωπίζονται με επιφύλαξη) και μόνο μία τυχαιοποιημένη κλινική μελέτη (TEMPRANO), που όμως κρίθηκε μέτριας ποιότητας [17]. Αυτή η πληροφορία είναι ιδιαίτερα σημαντική, αφού μόνο οι καλές τυχαιοποιημένες κλινικές μελέτες (Randomized Controlled Trial, RCT) μπορούν να δικαιολογήσουν μια αλλαγή θεραπευτικής ή προληπτικής στρατηγικής. Βεβαίως, μια δεύτερη RCT επιβεβαίωσε τα οφέλη της πρώιμης έναρξης cART, αν και δημοσιεύτηκε μεταγενέστερα, με αποτέλεσμα να μην συμπεριληφθεί στη συστηματική ανασκόπηση από όπου προέκυψαν οι τελευταίες οδηγίες του Π.Ο.Υ. Πρόκειται για τη μελέτη START, που όπως και η μελέτη HPTN 052, διεκόπη πρόωρα, αφού τα αποτελέσματα ήταν ήδη σαφώς υπέρ της πρώιμης έναρξης [18]. Ωστόσο, τα πράγματα δεν είναι τόσο απλά· η στατιστική σημαντικότητα δεν μεταφράζεται απαραίτητα σε κλινική σημαντικότητα ούτε και προεξοφλεί όφελος στο επίπεδο της δημόσιας υγείας και της οικονομίας πόρων. Η πληροφορία ότι η πρώιμη έναρξη της cART ελαττώνει κατά 57% τα σχετιζόμενα με AIDS συμβάντα, τα μη σχετιζόμενα με AIDS συμβάντα και τους θανάτους, το αποτέλεσμα δηλαδή της μελέτης START, πρέπει να διαβαστεί με επίγνωση του πόσο σπάνια είναι έτσι κι αλλιώς αυτά τα συμβάντα σε HIV+ άτομα με CD4+ >500/mm3. Σε απόλυτους αριθμούς, η κατά 57% μείωση των συμβάντων αυτών αποδίδει απλώς τη μείωσή τους από 4,1% σε 1,8%, δηλαδή πρόκειται για μια απόλυτη διαφορά της τάξης του 2,3%. Φυσικά, αν αναγάγουμε το 2,3% στον HIV+ πληθυσμό των δεκάδων εκατομμυρίων, αντιλαμβανόμαστε ότι μιλάμε για εκατομμύρια συμβάντα που μπορεί να προληφθούν με την πρώιμη έναρξη θεραπείας. Απαιτείται ωστόσο μια πολύ προσεκτική προσέγγιση, που θα λαμβάνει υπόψη της και τους σοβαρούς κινδύνους που συνοδεύουν την πρώιμη έναρξη σε επίπεδο συμμόρφωσης, συνέχισης της θεραπείας εφ’ όρου ζωής, ανεπιθύμητων ενεργειών των αντιρετροϊκών φαρμάκων, κόστους κ.λπ. Χρειάζονται δηλαδή νέες, κατάλληλα σχεδιασμένες τυχαιοποιημένες κλινικές μελέτες, μελέτες κόστους-οφέλους, περισσότερα δεδομένα μακροχρόνιας παρακολούθησης και καλύτερη ενημέρωση και εκπαίδευση των HIV+ ατόμων κατά τη διάγνωση σχετικά με τα οφέλη και τους κινδύνους της έναρξης cART. Όπως σημειώνεται και στις οδηγίες του Π.Ο.Υ., παρότι είναι αδιαμφισβήτητα ωφέλιμη η έναρξη cART όταν CD4+ ≤ 350/mm3 ή υπάρχει νόσος κλινικού σταδίου 3 ή 4, για τα ασυμπτωματικά HIV+ άτομα με CD4+ > 500/mm3 η προσέγγιση πρέπει να είναι εξατομικευμένη και να λαμβάνει υπόψη της τις ανάγκες και την ετοιμότητα του ατόμου.
Οι ελληνικές οδηγίες
Σύμφωνα με τις πιο πρόσφατες ελληνικές οδηγίες, αυτές του 2015, συστήνεται η έναρξη cART σε κάθε HIV+ άτομο με CD4+ ≤ 350/mm3 ή συμπτωματική λοίμωξη (δηλαδή, πλην σταδίου 1), ενώ σε ό,τι αφορά τα ασυμπτωματικά HIV+ άτομα με υψηλότερες τιμές CD4+ Τ-λεμφοκυττάρων η έναρξη της θεραπείας είναι προαιρετική και γίνεται σε συνεννόηση με τον πάσχοντα [19]. Σε γενικές γραμμές, οι ελληνικές οδηγίες είναι πιο συντηρητικές σε σχέση με εκείνες του Π.Ο.Υ., ωστόσο πρέπει να σημειωθεί ότι ακόμα και ο Π.Ο.Υ. που τολμά να συστήσει την έναρξη θεραπείας για ασυμπτωματικά άτομα σε υψηλότερες τιμές CD4+ τονίζει τη σημασία της εξατομίκευσης.
Κίνδυνος Πρώιμης Έναρξης
Παρότι είναι σαφές πως με τον χρόνο, οι ενδείξεις για την έναρξη αντιρετροϊκής αγωγής γίνονται ολοένα και λιγότερο συντηρητικές, η πρώιμη έναρξή της συνοδεύεται από σημαντικό κίνδυνο. Όπως είχε ήδη αναγνωριστεί στις οδηγίες του Π.Ο.Υ. του 2002, όσο αυξάνεται το χρονικό διάστημα της θεραπείας αυξάνεται και ο κίνδυνος μεταλλάξεων, που μπορεί να οδηγήσουν σε ανθεκτικά στελέχη του ιού. Εκδηλώνεται λοιπόν ανησυχία για τη μακροπρόθεσμη επίπτωση της πρώιμης έναρξης της αγωγής στη δημόσια υγεία. Πέραν τούτου, δεδομένου ότι το κόστος της θεραπείας είναι υψηλό και οι πόροι περιορισμένοι, υπάρχει πιθανότητα να εξαντλούνται οι πόροι κατά την κάλυψη ασυμπτωματικών ατόμων για τα οποία η θεραπεία δεν είναι απαραίτητη, με αποτέλεσμα να μένουν ακάλυπτοι εκείνοι για τους οποίους είναι απαραίτητη (AIDS, CD4+ ≤ 350/mm3 κ.λπ.).
Επιπλέον, καθώς πρόκειται για μια αγωγή που πρέπει να λαμβάνεται μία ή δύο φορές ημερησίως εφ’ όρου ζωής, υπάρχει αυξημένη πιθανότητα κακής συμμόρφωσης ως προς τη θεραπεία ή, χειρότερα, πρόωρου τερματισμού της. Ιδιαίτερα, αν συνυπάρχουν καταστάσεις όπως κατάχρηση αλκοόλ ή ναρκωτικών ουσιών και ψυχική νόσος.
Τέλος, σημαντικός είναι και ο κίνδυνος πρόωρης εξάντλησης των θεραπευτικών επιλογών. Στην πορεία της νόσου, οι ασθενείς μπορεί να χρειαστεί να αλλάξουν την αγωγή τους είτε σε έδαφος μη ανταπόκρισης ή θεραπευτικής αποτυχίας είτε σε έδαφος ανεπιθύμητων ενεργειών των αντιρετροϊκών φαρμάκων. Έτσι, μετά τη θεραπεία πρώτης γραμμής, ακολουθεί αυτή της δεύτερης γραμμής και, τέλος, της τρίτης γραμμής. Όσο αυξάνεται το χρονικό διάστημα της θεραπείας τόσο αυξάνεται ο κίνδυνος να εξαντληθούν οι θεραπευτικές επιλογές νωρίς, με τον ασθενή σε ηλικία μικρότερη του προσδόκιμού του.
Παρότι υπάρχουν έρευνες που δείχνουν πως τα οφέλη της πρώιμης έναρξης εξουδετερώνουν τους κινδύνους ακόμα και σε ασθενείς με κακή συμμόρφωση στη θεραπεία [20, 21], η επιφυλακτικότητα απέναντι στην πρώιμη έναρξη της αντιρετροϊκής αγωγής είναι, τουλάχιστον θεωρητικά, δικαιολογημένη.
Επίλογος και οικονομική πραγματικότητα
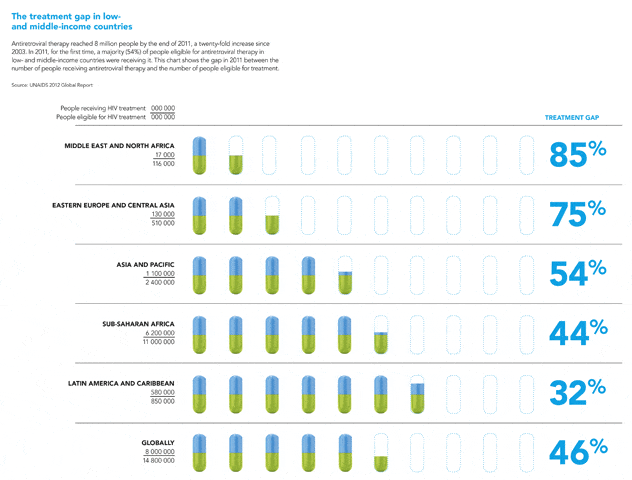
Δεδομένης της γεωγραφικής κατανομής της επιδημίας του HIV, είναι φυσικό πως στις περισσότερες χώρες με υψηλό επιπολασμό της νόσου, το κόστος της θεραπείας (αλλά και του ελέγχου που θα θέσει την ένδειξη έναρξης της θεραπείας) είναι απαγορευτικό. Μόλις το 2011, για πρώτη φορά, περισσότεροι από τους μισούς ασθενείς με ένδειξη έναρξης θεραπείας είχαν πρόσβαση σε αυτή [22]. Όπως φαίνεται και στην Εικόνα ΙΙ, η πρόσβαση στην αντιρετροϊκή θεραπεία είναι πολλαπλών ταχυτήτων. Υπό αυτό το πρίσμα, το ενδεχόμενο ο Π.Ο.Υ. να υιοθετήσει την ολοκληρωτική σύσταση της Διεθνούς Αντι-ιικής Εταιρείας για έναρξη της θεραπείας σε όλους τους HIV+ ασθενείς θα σήμαινε μεγάλο κόστος: θα χρειάζονταν χρήματα για ένα σύνολο 30.000.000 ασθενών· μάλιστα, ένα σύνολο με διαρκώς αυξανόμενο προσδόκιμο ζωής. Και παρότι η Διακήρυξη της Ντόχα (14 Νοεμβρίου 2001), με την περισσότερο ευέλικτη διαχείριση των κανόνων που διέπουν τα διπλώματα ευρεσιτεχνίας, επέτρεψε στις χώρες με χαμηλό και μεσαίο εισόδημα να αγοράσουν γενόσημα αντιρετροϊκά φάρμακα και να καθυστερήσουν την αποπληρωμή των δικαιωμάτων πνευματικής ιδιοκτησίας στις φαρμακευτικές εταιρείες παραγωγής, ρίχνοντας έτσι τις τιμές των αντιρετροϊκών φαρμάκων [23] και θεμελιώνοντας ―μαζί με διεθνείς πόρους― τους στόχους δημόσιας υγείας του Π.Ο.Υ., μένει να δούμε πώς η διεθνής κοινότητα θα μπορέσει να ανταποκριθεί σε τέτοιο ενδεχόμενο. Ειδικά, αν λάβει κανείς υπόψη του το υψηλό κόστος της θεραπείας δεύτερης ή και τρίτης γραμμής [23]· θεραπευτικά σχήματα που, με πρώιμη έναρξη θεραπείας, ίσως χρειάζεται όλο και μεγαλύτερο ποσοστό ασθενών στο μέλλον. Παρόλ’ αυτά, πιθανολογείται πως η ελαττωμένη νοσηρότητα και η ελαττωμένη επίπτωση της HIV λοίμωξης που πιστεύουμε ότι θα προκύψουν με την πρώιμη έναρξη της cART θα αποσβέσουν το κόστος της επένδυσης [17].
Σημειώσεις
¹Υπάρχουν δύο ειδών ιοί ανθρώπινης ανοσοανεπάρκειας, ο HIV-1 και ο HIV-2. Ο ΗΙV-1 είναι υπεύθυνος για την πλειονότητα των HIV λοιμώξεων κι έτσι όταν μιλάμε για «HIV», συνήθως μιλάμε για τον HIV-1. O HIV-2 εμφανίστηκε το 1986 στη Δυτική Αφρική, όπου και περιορίστηκε. Και παρότι λοιμώξεις με HIV-2 έχουν διαπιστωθεί και σε άλλα μέρη του κόσμου, συνήθως η μετάδοση έχει συμβεί στη Δυτική Αφρική ή από επαφές με Δυτικούς Αφρικανούς.
2Με τον όρο «γριππώδης συνδρομή» περιγράφεται κάθε σύνδρομο που μοιάζει με γρίππη (πυρετός, αδυναμία, βήχας, ρινική καταρροή, δακρύρροια, κεφαλαλγία, καρηβαρία, ασαφώς εντοπιζόμενα μυοσκελετικά άλγη κ.λπ.). Από την άλλη, ως «σύνδρομο λοιμώδους μονοπυρήνωσης» περιγράφονται οι περιπτώσεις που μοιάζουν με λοιμώδη μονοπυρήνωση (πυρετός, αδυναμία, φαρυγγίτιδα, λεμφαδενοπάθεια, σπληνομεγαλία, εξάνθημα κ.λπ.).
3«Καθοριστικά του AIDS Νοσήματα» καλούνται οι νοσολογικές οντότητες που ορίζουν Κλινικό Στάδιο 3 κατά CDC [7]. Δεν διαφέρουν από εκείνες που ορίζουν Κλινικό Στάδιο 4 κατά WHO [4].
4Ο HIV μεταδίδεται, μεταξύ άλλων, και με τον θηλασμό. Γι’ αυτό, στις αναπτυγμένες χώρες, η HIV Λοίμωξη της μητέρας αποτελεί αντένδειξη για θηλασμό. Ωστόσο, σε χώρες του Τρίτου Κόσμου, όπου δεν υπάρχει πρόσβαση σε τροποποιημένο γάλα (φόρμουλα) ή καθαρό νερό και ο μητρικός θηλασμός είναι ο μοναδικός τρόπος για να εξασφαλιστεί η επαρκής θρέψη του νεογνού και η παθητική του ανοσοποίηση, ο θηλασμός αποκτά κατ’ εξαίρεση ένδειξη. Σε αυτές τις περιπτώσεις, λοιπόν, προκειμένου να ελαττωθεί ο κίνδυνος μετάδοσης του ιού, οι μητέρες ή/και τα νεογνά λαμβάνουν αντιρετροϊκή θεραπεία [24].
Βιβλιογραφία
[1] Global AIDS Update 2016. UNAIDS Report. May 2016. http://www.who.int/hiv/pub/arv/global-aids-update-2016-pub/en/
[2] Closing the Gap: Increases in life expectancy among treated HIV-positive individuals in the United Stated and Canada. Samji H, Cescon A et al. PLoS One 2013 Dec 18;8(12):e81355.
[3] Prevention of HIV-1 Infection with Early Antiretroviral Therapy. The HPTN 052 Study Team. N Engl J Med 2011; 365:493-505 August 11, 2011.
[4] Who Case Definitions of HIV for Surveillance and Revised Clinical Staging and Immunological Classification of HIV-related Disease in Adults and Children, 2007.
[5] Guidelines for the Use of Antiretroviral Agents in HIV-Infected Adults and Adolescents. Department of Health and Human Services, February 4, 2002.
[6] Prognosis of HIV-1-infected patients starting highly active antiretroviral therapy: a collaborative analysis of prospective studies. Egger M. Lancet. 2002 Jul 13;360(9327):119-29.
[7] Revised Surveillance Case Definitions for HIV Infection Among Adults, Adolescents, and Children Aged <18 Months and for HIV Infection and AIDS Among Children Aged 18 Months to <13 Years — United States, 2008. December 5, 2008 / 57(RR10);1-8.
[8] Scaling Up Antiretroviral Therapy in Resource-Limited Settings: Treatment Guidelines For A Public Health Approach. 2003 Revision. WHO.
[9] Antiretroviral Therapy For HIV Infection in Adults and Adolescents: Recommendations for a public health approach. 2006 Revision. WHO.
[10] Antiretroviral Therapy For HIV Infection in Adults and Adolescents: Recommendations for a public health approach. 2010 Revision. WHO.
[11] When to initiate combined antiretroviral therapy to reduce mortality and AIDS-defining illness in HIV-infected persons in developed countries: an observational study. HIV- CAUSAL Collaboration. Ann Intern Med. 2011 Apr 19;154(8):509-15.
[12] Antiretroviral Treatment of Adult HIV Infection: 2012 Recommendations of the International Antiviral Society–USA Panel. JAMA. 2012;308(4):387-402.
[13] The Use of Antiretroviral Drugs for Treating and Preventing HIV Infection: Recommendations for a Public Health Approach. 2013 Revision. WHO.
[14] Early initiation of antiretroviral therapy in HIV-infected adults and adolescents: a systematic review. Anglemyer A, Rutherford GW, Easterbrook PJ, Horvath T, Vitória M, Jan M, Doherty MC. AIDS. 2014 Mar;28 Suppl 2:S105-18.
[15] Preexposure Prophylaxis for the Prevention of HIV Infection in the United States -2014: a Clinical Practice Guideline. CDC.
[16] Antiretroviral Treatment of Adult HIV Infection: 2014 Recommendations of the International Antiviral Society–USA Panel. JAMA. 2014;312(4):410-425.
[17] Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection. Recommendations for a public health approach – Second edition. WHO. June 2016. http://www.who.int/hiv/pub/arv/arv-2016/en/
[18] INSIGHT START Study Group, Lundgren JD, Babiker AG, Gordin F, Emery S, Grund B, Sharma S, Avihingsanon A, Cooper DA, Fätkenheuer G, Llibre JM, Molina JM, Munderi P, Schechter M, Wood R, Klingman KL, Collins S, Lane HC, Phillips AN, Neaton JD. Initiation of Antiretroviral Therapy in Early Asymptomatic HIV Infection. N Engl J Med. 2015 Aug 27;373(9):795-807.
[19] Κατευθυντήριες οδηγίες χορήγησης αντιρετροϊκής αγωγής σε ενήλικες και εφήβους. ΚΕΕΛΠΝΟ. Απρίλιος 2015. http://www.aids.org.gr/pdfs/ODHGIES_ANTIRETRIOKHS_AGOGHS.pdf
[20] Do Benefits of Earlier Antiretroviral Treatment Initiation Outweigh Harms for Individuals at Risk for Poor Adherence? R. Scott Braithwaite, Mark S. Roberts, […], and Amy C. Clin Infect Dis. Mar 15, 2009; 48(6): 822-826.
[21] Could Early Antiretroviral Therapy Entail More Risks than Benefits in sub-Saharan African HIV-Infected Adults? A Model-Based Analysis. Xavier Anglaret, MD, PhD, Callie A. Scott, MSc, […], and Kenneth A. Freedberg, MD, MSc. Antivir Ther. 2013; 18(1): 45–55.
[22] The treatment gap in low- and middle-income countries. 20 November 2012. UNAIDS. http://www.unaids.org/en/resources/infographics/20121120resultstreatmentgap/
[23] Untangling the Web of Antiretroviral Price Reductions. 14th Edition, July 2011. Médecins Sans Frontières.
[24] Breastfeeding and HIV-Infected Women in the United States: Harm Reduction Counseling Strategies. Judy Levison, Shannon Weber, and Deborah Cohan. Clinical Infectious Diseases 2014;59(2):304–9.
[25] Global Access of HIV Patients to HAART Therapy – What After Doha? Master’s Course in International Medicine – Health Crisis Management. Chasioti Yvoni, Athens, 2012.